Pletfrie standarder: Ekspertise i kontamineringskontrol i personlig pleje og kosmetik
Baseret på en artikel, der oprindeligt blev offentliggjort i juni 2025-udgaven af Personal Care Magazine.

Etabler en gentagelig og tydelig procedure for at sikre, at den visuelle rengøringskontrol vurderes korrekt og ensartet af forskellige operatører.
Forestil dig, at én enkelt fejl i din rengøringsprocedure kunne plette dit brands omdømme på blot få dage. Fra hvad der syntes at være et simpelt fejltrin i din rengørings- og desinficeringsprocedure (C&S), står du nu over for en produkttilbagekaldelse og pressemeddelelse for at advare forbrugerne, en formel årsagsanalyse og en korrigerende handlingsplan blandt mange andre ansvarsområder. De økonomiske og omdømmemæssige omkostninger er enorme, og potentielle FDA (USA's fødevare- og lægemiddelforvaltning)-fund kan øge byrden yderligere. Du har nu dedikeret timer, dage eller endda uger til at rette op på et problem, der let kunne have været forhindret med korrekt C&S-kontrol. I kosmetikverdenen handler sikring af pletfrit udstyr ikke kun om overholdelse - det handler om at beskytte forbrugernes tillid og sundhed.
For det meste kræver regler verden rundt, at produkter til personlig pleje og kosmetik ikke er forfalsket eller kontamineret. Producenten skal overholde disse regler ved at kontrollere kritiske trin i fremstillingsprocessen for at sikre, at kontaminering ikke forekommer. Der kan indføres forskellige kontroller i fremstillings- og emballeringsprocesserne, rengøring processer, medarbejderhygiejne, anlægshygiejne, råvarekontrol og uddannelse af medarbejdere for blot at nævne nogle få. Frigivelsen af udkastet til nuværende god fremstillingspraksis (cGMP'er) i Modernization of Cosmetics Regulation Act (MoCRA) afventer stadig, og med det kommer spekulationer om, hvad der vil eller ikke vil være påkrævet. Der kan henvises til den internationale standard for GMP'er til kosmetik, ISO 22716:2007, som en indikation af potentielle retningslinjer, der kan påvirke udkastet til MoCRA GMP'erne. For eksempel kræver ISO 22716:2007 - 4.10.3 & 4.10.4 specifikke rengørings- og/eller desinfektionsmidler, hvis effektivitet verificeres, og vælges og anvendes i henhold til de specifikke behov i hvert facilitetsområde. Med andre ord kan forskellige områder af dit anlæg kræve forskellige rengørings-SOP'er, og hver SOP's effektivitet skal verificeres. Som et andet eksempel beskriver ISO 22716:2007 - 7.2 vigtigheden af dokumentation, sporbarhed, kvalitetskontrol og batchstyring, blandt andre krav. Dette understreger presset på branchens bevægelse mod 'First Time Right' (FTR)-ideologier, som skal sikre, at driften altid er klar til revision, og at produkterne fremstilles og leveres i overensstemmelse med specifikationerne.
I sidste ende hjælper disse cGMP-retningslinjer med at mindske risikoen for kontaminering og giver virksomhederne tillid til, at de leverer sikre kvalitetsprodukter til deres forbrugere. Det skal anerkendes, at enhver ny GMP kan være skræmmende i starten. Da rengøring og sanitering (C&S) er en vigtig del af GMP, vil denne artikel give dig en overordnet gennemgang af risiciene og bedste praksis for rengøringsprocedurer for kritisk procesudstyr.
Omkostningerne ved beskidt udstyr
I den digitalt forbundne verden, vi lever i, kan en virksomheds brand inden for få dage blive negativt påvirket via sociale medier, hvis produktfejl når ud til forbrugerne. På samme måde kan rapporter om lovgivningsmæssige revisionsresultater eller en tilbagekaldelse skade brandets image. Disse defekter eller revisionsresultater kan have mange årsager, herunder rester overført fra den tidligere produktion på grund af utilstrækkelig rengøring eller smags- og viskositetsændringer på grund af mikrobiologisk forurening. I sidste ende gør producenterne rent for at minimere risikoen for produktforurening. Kontamineringstyper omfatter krydskontaminering af produkter, krydskontaminering med aktive stoffer, mikrobiel kontaminering eller endda kontaminering fra rengøringsmidler. I betragtning af disse risici er det afgørende at forstå de standarder for renlighed, der kræves for at sikre produktsikkerhed og -kvalitet. Dette bringer os til spørgsmålet: "Hvor rent er rent nok?
Hvor rent er rent nok?
Hvor meget der skal rengøres for at undgå kontaminering virker subjektivt og åbent for fortolkning. Til overvejelse i diskussionen kan rengøringsniveauer vurderes ud fra tre grader af renhed: visuelt rent, restfri rent og mikrobiologisk rent. Selvom disse kategorier af renlighed er relaterede, er hver især forbundet med forskellige niveauer af forbrugerrisiko. Tilsynsorganer, der har til opgave at sikre forbrugernes sikkerhed, har anvist en vis vejledning. De følgende afsnit vil undersøge hvert niveau, de tilknyttede risici og potentielle løsninger.
1. Synligt rent
ISO leverer en rengøringsstandard for branchen, der taler om "visuel renlighed" i ISO 22716 - 2007: Cosmetics-Good Manufacturing Practices (GMP)2, hvor rengøring beskrives som "adskillelse og eliminering af generelt synligt snavs fra en overflade" (afsnit 2.8). Denne standard foreskriver, at al synligt snavs skal fjernes fra udstyrs overflader.
Af alle typer kontaminering synes denne standard mest ligetil at opnå og bekræfte; I praksis er dette imidlertid ikke altid tilfældet. Der kan være tvetydighed i at definere "basistilstanden" eller udgangspunktet. For eksempel, hvad hvis tanken er rusten, ru eller på en eller anden måde beskadiget, sådan at ingen husker den smukke sølvglans fra det nye rustfri stål? Hvordan ville man etablere en standard for synligt rent? Tankrensning eller -passivering kan udføres i en sådan situation for at bringe udstyret tilbage til en "grundtilstand" eller en tæt på ny tilstand. Alternativt kan en kvalitetsgruppe og en produktionsgruppe gennem tests (rester, mikrobiel) og risikovurdering afstemme i forhold til den bedste aktuelle tilstand og en ny baseline.
Så hvordan måler man synligt rent? Synligt rent er en testmetode, der kræver en procedure, standardisering og måske kalibrering. Lad os undersøge tre nøglevariabler, der hjælper med at definere, hvad der betragtes som visuelt rent: lysforhold, overfladeforhold og måleinstrumentet.
Belysning, eller mangel på lys, kan påvirke evnen til at se overfladen tydeligt. Således skal en C &S-inspektionsprocedure omfatte en belysningsdefinition, der specificerer lyskilde, pæretype, belysningsvinkel og så videre. Vedligeholdelse af den lyskilde kan også være nødvendig, da pærens tilstand kan forringes med tiden. Nogle gange kan en forebyggende vedligeholdelsesplan for lyskilden være nødvendig.
Tilstanden af den inspicerede overflade er også afgørende. For eksempel kan en våd overflade se anderledes ud end en tør overflade og kan skjule tilstedeværelsen af rester af snavs. Proceduren skal således specificere overfladens tilstand, dvs. om overfladen er våd eller tør, for inspektion.
Operatøren er det primære "instrument" eller testenhed i en vurdering af synligt rent. En operatør skal vurderes eller kvalificeres som i stand til at udføre testen. Synsstyrke, korrigerende linser og evnen til at skelne farver kan være afgørende for at kvalificere en tekniker til en vurdering af visuelt rent. Når kvalifikationen er fastslået, bør teknikeren trænes i korrekte inspektionsteknikker i følge den skriftlige procedure.
Når først disse procedurekrav er defineret, skal succeskriterier for testen fastlægges. Da intet numerisk testresultat er knyttet til visuel vurdering, er en visuel standard nødvendig for at sikre konsekvent måling i forhold til succeskriterierne. Dette opnås ofte gennem en visuel standard skabt med billeder af acceptable vs. ikke-acceptable forhold. Resultaterne skal dokumenteres efter hver rengøring. Disse visuelle standarder hjælper med at mindske den risiko, der følger med, når flere kvalificerede operatører udfører den visuelle inspektion. Selvom papirbaserede og digitale formater er acceptable til opbevaring af disse procedurer, er der mange fordele ved at bruge et digitalt format. Disse fordele omfatter, men er ikke begrænset til, en mere interaktiv og engagerende træning af operatørerne, robust dokumentation, samt historisk datasporbarhed til revisionsberedskab.
2. Restfri ren
Selvom udstyret er rengjort efter en "synligt rent"-standard, kan rester til stede i niveauer, der ikke er synlige, påvirke forbrugernes sikkerhed. For eksempel er nogle aktive stoffer, såsom ingredienser i kemiske solfiltre, ikke visuelt påviselige. Vaskemidler kan også efterlade rester, der påvirker produktkvaliteten, hvis de ikke afskylles tilstrækkeligt, hvilket muligvis ikke kan påvises ved visuel inspektion.
Det er ikke økonomisk gunstigt for producenterne at fjerne alle sporbare niveauer af produkt, aktive stoffer og vaskemiddel for at sikre en ren overflade, da der kan kræves store mængder tid og vand. Afhængigt af branchen kan tilsynsmyndigheder tage en risikobaseret tilgang, der kræver, at rester reduceres til et "sikkert niveau" til kundebrug. Ofte er dette "sikre niveau" baseret på en toksikologisk vurdering, der sikrer, at den resterende mængde, der overføres til næste batch, ligger langt under et niveau, hvor der kan observeres en effekt eller en opstået bivirkning. Dette kræver, at producenterne kender de rester, der kan være til stede, et sikkert og acceptabelt restniveau, en testmetode til at verificere restkoncentrationen og en rengøringsproces, der pålideligt fjerner produktet, aktive stoffer og vaskemiddel til det sikre niveau. En kosmetisk producent kender deres formulering, så de kender de aktive stoffer eller formulerede ingredienser, der kan blive tilbage som rester, samt den tilknyttede aktivitet eller toksicitet. De har typisk en testmetode, der allerede er udviklet for den aktive ingrediens, da de sandsynligvis tester den endelige formel for at bekræfte, at den er inden for specifikationerne. Denne testmetode skal muligvis verificeres eller ændres for at måle de mindste restaktive stoffer efter rengøring nøjagtigt. Ofte kan en uspecifik testmetode som TOC-testen (Total Organic Carbon) bekræfte, at ikke-aktive formuleringingredienser er fjernet.
Den største ubekendte faktor for kosmetikproducenter kan være det anvendte rengøringsmiddel. En velrenommeret leverandør vil være i stand til at dele toksicitetsoplysningerne for vaskemidlet og passende testmetoder til bestemmelse af restkoncentrationer. Inden for industrien kan testmetoder være specifikke (identifikation af den bestemte kemiske komponent) eller ikke-specifikke (angiver tilstedeværelsen af en rest, men ikke det pågældende kemikalie) baseret på en toksicitetsrisikovurdering. Ofte er rengøringsmidler, der anvendes i kosmetikapplikationer, lavrisikoprodukter og kan testes ved ikke-specifikke metoder. Eksempler inkluderer TOC-testen (Total Organic Carbon), ledningsevne, pH osv. I alle disse tilfælde kræves laboratoriearbejde for at give en korrelation eller oversættelse fra det uspecifikke metoderesultat til det faktiske restniveau. Vaskemiddelproducenten bør kunne hjælpe med dette forløb.
Mens opnåelse af resterende renlighed er afgørende for at eliminere skjulte forurenende stoffer, er det lige så vigtigt at tackle de mikrobielle trusler, der kan kompromittere produktsikkerheden. Dette bringer os til det sidste niveau af renlighed: at sikre, at udstyret er mikrobielt rent.
3. Mikrobielt rent
Mikrobiel kontaminering forårsaget af biobelastning i udstyret bliver en stadig større bekymring og et voksende fokusområde i kosmetikindustrien. Det er nødvendigt at præcisere begreberne, før vi undersøger mulighederne for at kontrollere mikrobiel kontaminering. To udtryk, der forvirrer den globale verden - desinficering og desinfektion. I EPA - og USP-standarder kaldes reduktion af mikrobiel belastning desinficering, mens desinfektion defineres som ødelæggende eller irreversibelt inaktiverende mikroorganismer. I denne artikel vil vi bruge udtrykket desinficering til at betyde reduktion af mikrobiel belastning til ønskede niveauer, uanset applikationens geografiske placering.
Når kriterier for synlig renhed og restkoncentrationer er blevet opfyldt, er der fortsat basis for mikrobielle rester på udstyr, der kan kontaminere et kosmetisk produkt. Hvis mikrobiel kontaminering er ekstrem, som i et slimet, misfarvet område, der indikerer tilstedeværelse af biofilm, kan en visuel inspektion opdage problemet. Ofte opdages mikrobiel kontaminering kun gennem test af færdige produkter, med høje mikrotal, der resulterer i batchafvisning. Selvom historikken ikke viser nogen problemer med mikrobiel kontaminering for produkter fremstillet på et anlæg, bevæger de nuværende produkttrends sig mod mere naturlige ingredienser, hvilket kan øge risikoen for at introducere hidtil uset mikrobiel flora. Derudover indskrænkes mulighederne for konserveringsmidler, da EU fjerner konserveringsmidler til brug i kosmetiske produkter, hvilket betyder mindre sikkerhed i formuleringen for at modvirke mikrobiel vækst og kontaminering.

Uden ordentlige rengørings- og desinficeringsprocedurer risikerer dit udstyr mikrobiel vækst, hvilket kan vise sig som biofilm på indersiden af dit udstyr
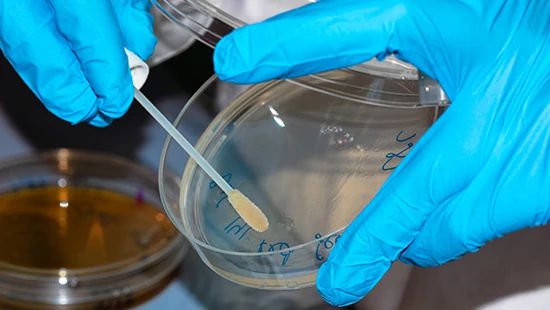
Mikropodning er en almindelig metode til at teste mikrobielle rester.
Mikrobielle rester kan måles med enten mikropodepinde eller skyllevandsprøver, afhængigt af udstyrets design og tilstand. Der er særlige udfordringer med testning af mikrobielle rester, primært relateret til adgang til prøvepunkter. Ofte er de områder i udstyret, der har størst risiko for mikrovækst, områder, der ikke er let tilgængelige, såsom rør, udstyrssamlinger eller i nogle tilfælde udstyrsoverflader, der er beskadiget af ridser eller tæring. Disse områder, der er svære at få adgang til til prøveudtagning, er også de sværeste at rense effektivt, hvilket øger risikoen.
Den primære metode til at kontrollere mikrobielle rester på rengjort udstyr er gennem et desinficeringstrin. Producenter af personlig pleje og kosmetik har historisk brugt termisk desinfektion til at reducere mikrobielle rester. Trends indenfor formler som nævnt ovenfor øger vigtigheden af at opretholde god mikrobiel kontrol i produktionsudstyret. Yderligere pres for at kontrollere omkostningerne og reducere energiforbruget resulterer i, at virksomheder bevæger sig fra den ofte brugte varmtvandsdesinficering til kemisk desinficering. Tilliden til, at den termiske proces er effektiv og fungerer i den validerede tilstand, afhænger i høj grad af temperatur og tid for alle kontaktpunkter på udstyret. Kemisk desinficerin bliver mere og mere populær med sikker mikrobiologisk effektivitet valideret ved hjælp af et specifikt produkt, koncentration og kontakttid - ofte ved omgivende temperaturer og i blot et par minutter.
Opsummering
Det er af afgørende betydning for forbrugernes sundhed og sikkerhed, at produkter til personlig pleje og kosmetik fremstilles i et miljø uden kontaminering. Et vigtigt skridt, producenten kan tage, er at udvikle et rengøring-s og desinficrinsprogram, der effektivt fjerner kontaminering fra produktionen. Disse kontaminanter kan være rester fra produkter (aktive eller ej), rengøringsmidler eller mikrobiel belastning. Rengøring til en "synligt ren" standard er bydende nødvendigt og ikke til forhandling som udgangspunkt. Udvikling af standarden - processen, acceptgrænser og træning - er kritisk.
Vi er kommet frem til, at det måske ikke er nok at opnå "synligt rent". Rester, der ikke er synlige, såsom rester af aktive stoffer, rester af vaskemidler eller mikrobiobyrde, kan bidrage til kontaminering, der påvirker produktkvaliteten. Rengørings- og desinficeringsprogrammer skal behandle alle disse resttyper nøje for at give tillid til, at produktkvaliteten ikke påvirkes.
For at sikre, at dine produkter opfylder de højeste standarder for renlighed og sikkerhed, er et samarbejde med eksperter, der specialiserer sig i kontamineringskontrol, en overvejelse værd. Dette kan beskytte dit brands omdømme, beskytte forbrugernes sundhed og være på forkant med lovkravene. Vent ikke på et kontamineringsproblem - tag proaktive skridt nu for at implementere et robust rengørings- og desinfektionsprogram.

Overvind udfordringer på produktionsgulvet
Ecolab kan optimere dine processer for produktion af personlig pleje.
Opnå betydelige tids- og omkostningsbesparelser.
Referencer
- Bilag 15 til EU's GMP-retningslinjer siger: "Grænseværdier for overførsel af produktrester bør baseres på en toksikologisk evaluering. Begrundelsen for de valgte grænseværdier bør dokumenteres i en risikovurdering, der omfatter alle understøttende referencer."
- Kilde: https://www.epa.gov/pesticide-registration/pesticide-registration-manual-chapter-4-additional-considerations
- Kilde: USP kapitel 1072